A história da química está muito ligada a evolução da humanidade, muito antes de entender os conceitos químicos a humanidade já o utilizavam. Há indícios que os conhecimentos dessa ciência surgirão junto com a descoberta do fogo.
Veremos que ela surgiu de forma experimental, através de observações junto com os filósofos. Vamos ver mais sobre isso:
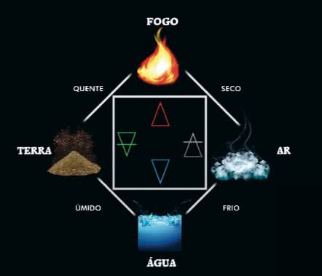
Aristóteles pensava que a natureza era composta por elementos básicos (ar, terra, fogo e água) portadores de propriedades fundamentais que caraterizavam qualquer substância. Paralelamente, surgia as teoria da existência do átomo.
Leucipo e Demócrito em 400 a.c. Eles pensavam que a matéria não poderia ser dívida infinita vez, havia um limite e esse limite ficou conhecido como átomo.
O desenvolvimento de um fenômeno importante na história da química ocorreram entre os séculos III a.C e XVI d.C, esse movimento foi chamado de alquimia. Nesse momento pretendia-se desenvolver um método hipotético que poderia transformar qualquer metal em ouro e o explicar a existência da vida. Na pesquisa alquimia, novos produtos químicos e métodos de separação de elementos químicos foram desenvolvidos. Desta forma, o pilar básico do futuro desenvolvimento da química experimental foi estabelecido. O cientista irlandês Robert Boyle é considerado por muitos o pioneiro da química moderna porque conduziu experimentos planejados em meados do século XVII e os generalizou por meio desses experimentos. Apesar das vantagens de Boyle, muitas pessoas acreditam que o francês Antoine Laurent Lavoisier, que viveu no século XVIII, foi o pai da química, devido a importância de seus experimentos, entre eles o de conservação da massa, que estabelecida que a massa se conserva em uma reação química quando a mesma ocorre em recipiente fechado, esse foi considerado o marco do estabelecimento da química moderna, ocasionando a chamada Revolução Química. Esse estudo precederam as observações feitas por John Dalton, no início do século XIX, que foi o primeiro modelo atômico proposto.
John Dalton (1766 -1844) foi um químico, meteorologista e físico britânicos que trouxe a ideia de átomo, massa atômica, pressão parciais. A química passou por um grande desenvolvimento teórico e metodológico no século XX, especialmente através do estabelecimento da mecânica quântica, espectroscopia e métodos de síntese orgânica, que promoveram a descoberta de novos fármacos e a determinação de estruturas químicas moleculares, como o ácido desoxirribonucléico e teorias existentes.
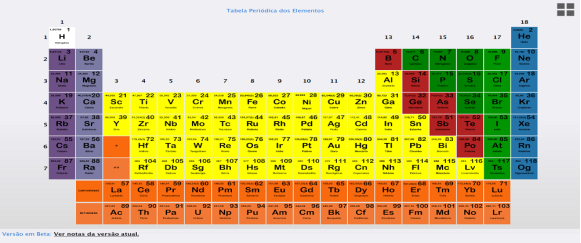
Após esse desenvolvimento começo-se a busca por novos elementos e teve-se o desenvolvimento da tabela periódica.
A primeira ideia de agrupamento dos elementos surgiu em 1817, com Johann Wolfgang Döbereiner (1780-1849), ele percebeu que os elementos semelhantes, se comportavam de forma similar que outros, dessa forma eles forma agrupados, esse modelo ficou conhecido como Tríades.
Por volta de 1862, quando Alexander Béguyer de Chancourtois (1820-1886), organizou os elementos dividido a um cilindro em 16 colunas e inúmeras horizontais. Em 1864 John A. R. Newlands (1838-1898) classificou os elementos pela ordem crescente de massa atômica em grupos de 7 dispostos lado a lado, ele havia percebido que as propriedades eram semelhantes ao primeiro e oitavo elementos – a contar da esquerda para a direita. Assim, os elementos que seguem a mesma linha vertical possuem as mesmas características químicas, como o lítio, o sódio e o potássio; o magnésio e o cálcio. Dois cientistas trabalharam isoladamente e chegaram a resultados semelhantes são eles Julius Lothar Meyer (1830-1895) e Dmitri Ivanovitch Mendeleev (1834-1907). Mendeleev propões que os elementos poderiam ser classificados segundo a sua massa atômica. Ele afirmava que as propriedades dos elementos são uma função periódica de suas massas atômicas.
Em 1913 Henry G. L. Moseley propos algumas modificalções no modelo de Mendelev e foi estabelecida a tabela periodica atual. A tabela periódica atual não é uma cópia do que Mendeleiev propôs, ela foi aperfeiçoada. Não pela aparição de elementos que ocupam os espaços vazios destinados a eles, mas por causa de um conceito estabelecido em 1913: o número atômico.
Em 1913 essa tabela recebeu algumas atualizações, feitas por Henry Moseley que organizou os elementos em ordem de número atômico dos elementos químicos. William Ramsay (1852- 1916), contribui com a formação da da tabela periódica sendo o descobridor de elementos como o neônio, argônio, criptônio e xenônio, que formam junto com os elementos hélio e radônio os gases nobres, que é uma família pertencente a Tabela Periódica.
Outra contribuição importante foi a de Glenn Seaborg (1912-1999) que descobriu os elementos transurânicos (do número 94 ao 102) e em 1944 propôs a colocação da série dos actinídeos abaixo da série dos lantanídios.
A bioquímica, anteriormente conhecida como biologia ou fisioquímica, apareceu nos fisiologistas e químicos do século 19 no estudo de compostos e transformações químicas em humanos e plantas. O termo bioquímica foi desenvolvido por químicos e alemães. proposto por Carl Neuberg (1877-1956) em 1903, embora no século 19 grandes pesquisadores como Wohler, Liebig, Química Pasteur e Claude Bernard estudassem a química da vida com outros nomes. Com a Segunda Guerra Mundial, o mundo entrou na era atômica, marcada pela descoberta dos elementos transurânicos e pelos avanços da radioquímica. A disponibilidade de isótopos permitiu a realização de importantes experimentos sobre a dinâmica e comportamento mecânico de compostos inorgânicos, que Henry Taube racionalizou em 1949 com base na teoria da ligação.
A química moderna traz o estudo de partículas elementares, átomos, moléculas, matéria e outros agregados de matéria. Matéria é tudo o que ocupa espaço e tem massa estática (ou massa constante). É o termo geral para as substâncias que constituem todos os objetos físicos.Geralmente, a matéria inclui átomos e outras partículas com massa. Algumas pessoas dizem que massa é a quantidade de matéria em um objeto e volume é a quantidade de espaço que o objeto ocupa, mas esta definição confunde massa e matéria.Eles não são a mesma coisa. Diferentes campos usam o termo de maneiras diferentes, às vezes até incompatíveis; embora o termo “qualidade” seja claramente definido, o termo “substância” não tem um significado cientificamente unificado. As substâncias existem principalmente em formas sólidas, líquidas e gasosas, isoladas ou combinadas.



Comentários